
①将a、b、c三种物质的饱和溶液从t2℃降温到t1℃,所得溶液均为t1℃时的饱和溶液
②将等质量的a、c两种物质配制成t2℃时的饱和溶液,c物质需要溶剂的质量多
③将a、b、c三种物质的饱和溶液从t2℃降温到t1℃,析出晶体的质量关系为a>b>c
④将t2℃时,等质量的a、b、c三种物质的饱和溶液,先蒸发等质量的水,再降温到t1℃,所得溶液的质量关系为c>b>a
⑤将a溶液由状态M点变为状态N点的方法是先降温到t1℃,再升温到t2℃
用溶质质量分数为6%的氯化钠溶液(密度约为1.04g/cm3),配制溶质质量分数为5%的氯化钠溶液60克。
计算需要6%的氯化钠溶液的体积是。(结果保留整数)
化学兴趣小组发现,实验室有一瓶装满生石灰的塑料瓶已经膨胀且破裂。
为探究破裂处生石灰变质的情况,同学们设计了如下实验。
实验燥作 | 实验现象 | 实验结论 | |
① | 取少量瓶中破裂处的白色固体于烧杯中,加入足量的水,用手触摸烧杯外壁,然后过滤,得到滤渣和滤液 | 烧杯壁无发热现象 | |
② | 取①中少量滤液于试管中,向其中加入一定量的Na2CO3溶液 | 有Ca(OH)2 | |
③ | 取①中少许滤渣于试管中,向其中加入适量的稀盐酸 | 有气泡产生 |
实验结论:由上述实验可确定所取白色固体的成分。
④将②③两支试管中所有物质倒入一洁净干燥的烧杯中静置,则上层清液中一定含有的离子是。(填离子符号)
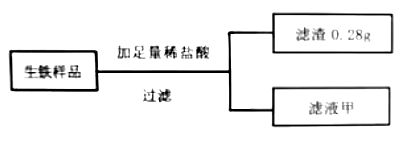
生铁出现锈蚀现象的原因是。
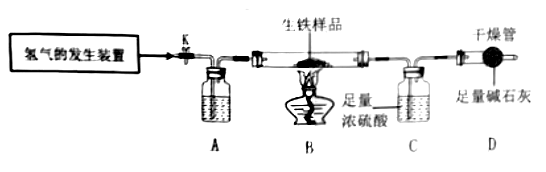
A装置瓶中盛放的试剂是。(填物质名称)
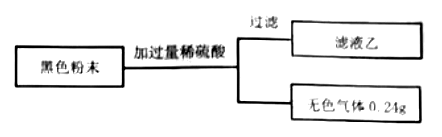
通过以上实验可得出,生铁中己锈蚀的铁的质量是,生铁粉末锈蚀前的含碳量是,有同学认为,由上述实验得出的已锈蚀的铁的质量可能存在误差,理由是。
