| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | CO2 | CO | 将混合气体通过灼热的CuO |
| B | NaCl | 泥沙 | 加水溶解、过滤、蒸发 |
| C | Cu粉 | Fe粉 | 用磁铁吸出 |
| D | KCl | KClO3 | 加入少量MnO2 , 加热 |
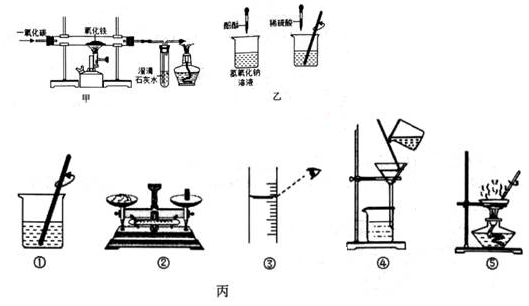
①实验步骤包括:a 计算产率,b 过滤,c 溶解,d 蒸发,e 称量。实验步骤的正确顺序是:e,,a(填写编号)。
②最后得到的精盐属于(填“混合物”或“纯净物”。)
③已知:产率= ×100%,某实验小组计算出的产率比其他组的产率低,你认为有哪些原因:。
①a.计算产率,b.过滤,c.溶解,d.蒸发,e.称量粗盐,f.称量精盐。实验步骤的正确顺序是:、a(填编号)。
②称量时正确的操作次序是(填字母序号)。
a.校正,b.去皮,c.放称量纸,d.放食盐,e.读数
③过滤时用到的玻璃仪器有玻璃棒、烧杯、,其中玻璃棒的作用是。实验过程中发现过滤两次滤液仍然浑浊,可能的原因是(写一点)。
④最后得到的精盐属于(填“混合物”或“纯净物”)。
|
组别 |
1 |
2 |
3 |
4 |
|
产率 |
75% |
65% |
88% |
72% |
|
教师评价 |
偏低 |
偏低 |
偏高 |
偏低 |
⑤已知:产率= ×100%。各小组的产率及评价如下,对造成产率偏高或偏低的原因分析,正确的是。
A.第1组:烧杯里的食盐未溶解完就开始过滤
B.第2组:没有蒸发干,精盐中仍然有水分
C.第3组:滤液浑浊就开始蒸发
D.第4组:过滤时滤液高于滤纸的边缘


A食盐没有全部溶解即过滤 B蒸发时食盐飞溅剧烈
C蒸发后,所得精盐很潮湿 D器皿上沾有的精盐没全部转移到称量纸上
称取粗盐样品W克,称量时应在托盘上各先后(填“放称量纸”、“按去皮键”)。

(实验名称)粗盐的提纯
(查阅资料)
①粗盐中含有泥沙及少量可溶性MgCl2、CaCl2、Na2SO4等杂质。
②Ba(OH)2是一种易溶于水的强碱。
(主要玻璃仪器)量筒、烧杯、漏斗、玻璃棒、胶头滴管、酒精灯
(主要试剂)粗盐样品、稀盐酸、BaCl2溶液,NaOH溶液,Na2CO3溶液,蒸馏水
|
步骤及目的 |
过程及说明 |
|
一、去除粗盐 中的泥沙 |
1.称取粗盐样品10.0g,用蒸馏水充分溶解 2.过滤去除泥沙的溶液I 以上两步操作中均需要使用到玻璃棒,玻璃棒的作用分别是:溶解时:; 过滤时:。 |
|
二、去除可溶 性杂质 |
将溶液I按如图流程图进行处理: 1、加入“过量NaOH溶液时”,发生反应的化学方程式是。 2、过滤后,所得的滤渣成分有种。 3、判断“稀盐酸适量”的方法是。 |
| 三、获得产品 | 将溶液Ⅱ注入(填仪器名称)中,蒸发结晶,观察到,停止加热,利用余热蒸干。装置完全冷却后,获得干燥的产品9.4g。 |
| 四、数据处理 | 该粗盐样品中氯化钠的质量分数是94% |
实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是。
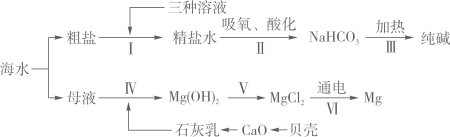
a.稍过量的Na2CO3溶液
b.稍过量的BaCl2溶液
c.稍过量的NaOH溶液