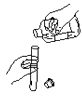
 倾倒液体
B .
倾倒液体
B . 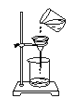 过滤
C .
过滤
C . 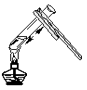 加热液体
D .
加热液体
D . 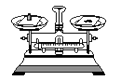 称量固体
称量固体

| 编号 | A | B | C | D |
| 实验设计 | | | | |
| 实验结论 | 二氧化碳能溶于水 | 化学反应前后物质的总质量不变 | 水是由氢气和氧气组成 | MnO2能加快H2O2反应速率 |
人工树叶可以自主呼吸,像普通树叶那样工作,能利用太阳能和催化剂产生化学反应,将水转化成氢气和氧气。研究表明,相对于普通树叶,它的“工作”效率提高了49%,需要的却仅仅是一点阳光、水和二氧化碳。其原理是利用蚕丝纤维的稳定性,从普通植物中提取出叶绿体浸入蚕丝材料中,最终可获得一片完全能够自主呼吸的树叶。它更轻,低耗能,并且生成氧气的效率却更高。
除此之外, “人工树叶”能够截获阳光中的能力,并转化为可用来驱动起床发动机的液体燃料。利用这种新型叶子中使用了一种酶,在与二氧化碳结合中可形成异丙醇(C3H8O),异丙醇可作为燃料使用。
人工树叶不仅可以用来制作灯具,照明的同时释放氧气,还可以挂上墙壁,用它做电视墙,家中就是一个天然的氧吧!建筑物的幕墙,可以作为外部空气的过滤器,人们在建筑物内呼吸到的是完全新鲜的氧气。这种神奇的新材料可以给执行长时间太空使命的宇航员提供稳定的氧气来源,甚至帮助人类依据新的星球。

回答下列问题:
(提出问题)影响该反应反应速率的因素有哪些?
(作出猜想)影响该反应反应速率的因素有温度、催化剂、硫酸的浓度等。
(查阅资料)硫酸锰(MnSO4)可作该反应的催化剂。
(进行实验)取A、B、C、D 4支试管,每支试管中分别加入4mL 0.08% 的KMnO4 溶液、0.4 mL 的硫酸、1mL 0.09% 的 H2C2O4 溶液。

(实验记录)
| 序号 | 所滴硫酸浓度 | 温度 | 催化剂 | 高锰酸钾完全褪色时间 |
| A | 98% | 室温 | 无 | 72s |
| B | 65% | 室温 | 无 | 129s |
| C | 65% | 50℃ | 无 | 16s |
| D | 65% | 室温 | MnSO4 | 112s |
草酸使高锰酸钾溶液褪色反应的化学方程式如下,请在横线上补全方程式。
2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10+ 8H2O
影响该反应反应速率的因素除温度、催化剂、硫酸的浓度外,还可能有。